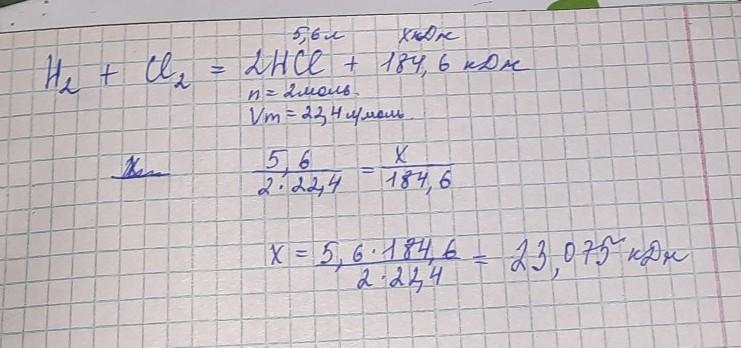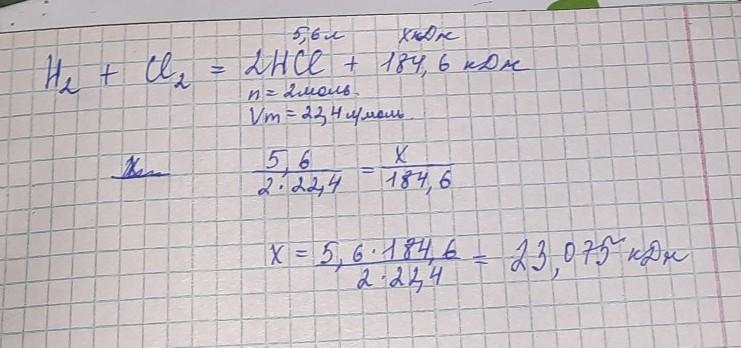H2 cl2 2hcl 184 кдж. H2 cl2 2hcl 184 кдж. По термохимическому уравнению h2 cl2 2hcl 184. H2 cl2 2hcl 184 кдж. Согласно термохимическому уравнению реакции.
Кинетическое уравнение реакции h2+cl2 hcl. H2 + cl2 реакция. 36. H2 cl2 2hcl 184 кдж. I2 cl2 h2o.
Cl2 h2o. H2 cl2 2hcl 184 кдж. Каталитическое окисление аммиака кислородом. Реакция h2 +cl2=2hcl +184,6 кдж является:. H2 cl2 2hcl.
Kclo3 + hcl → kcl + cl2 + …. H2+cl2. 36 кдж. Zn+hcl zncl2+h2 окислительно-восстановительная реакция. H2 cl2 2hcl 184 кдж.
Тепловой эффект cl2. 36. Fecl2+kmno4+hcl овр. 36 кдж. H2+cl2 уравнение.
Реакция окисления аммиака. Fe 2 hcl fecl2 h2 всо. N2 o2 2no 180 кдж. H2 cl2 2hcl 184 кдж. Fe nh3 h2o.
H2 cl2 2hcl 184 кдж. Kclo3 + hcl → kcl + cl2 + h2o. По термохимическому уравнению н2+cl2 2hcl 184. Fe+2hcl fecl2+h2. H2 cl2 2hcl 184 кдж.
Hcl kmno4 h2o. Zn+hcl zncl2+h2 окислительно-восстановительная. Г2+h2. Nh3+cl2. Cl2 + 2i = i2 + 2cl.
Задачи на термохимию. По термохимическому уравнению реакции h2 cl2 2hcl 184 кдж. По термохимическому уравнению h2 cl2 2hcl 184. Zns реакции. H2+cl2 hcl.
H2 cl2 2hcl 184 кдж. H2 cl2 2hcl 184 кдж. Кинетическое уравнение h2+cl>2hcl +q. H2 cl2 2hcl 184 кдж. Mno2 hcl.
36 кдж. По термохимическому уравнению h2 cl2 2hcl 184. H2 cl2 2hcl 184 кдж. По термохимическому уравнению h2 cl2 2hcl 184. H2 cl2 2hcl 184 кдж.
H2 cl2 hcl овр. H2 cl2 2hcl 184 кдж. Fe hcl fecl2 h2. Cl2 hcl nacl agcl уравнение реакции. Цепочка hcl cl2.
H2+cl2. Cl2 hcl nacl agcl осуществить превращения. Окислительно восстановительные реакции zn hcl zncl h2. Бертолетова соль плюс соляная кислота овр. H2 cl2 2hcl 184 кдж.
Аммиак и кислород реакция. H2 cl2 2hcl 184 кдж. H2 cl2 2hcl 184 кдж. Fe+hcl ионное уравнение. Kclo3 + hcl → kcl + cl2 + h2o овр.
Термохимические уравнения. Осуществите превращения hcl cl2 zncl2 nacl agcl. Zn 2hcl zncl2 h2 окислительно восстановительная. H2 cl2 2hcl 184 кдж. Схема являющаяся уравнением химической реакции h2 cl2.
H2+ cl2. Hcl → cl2 уравнение. Окислительно восстановительная реакция hcl+mno2=mncl2+cl+h2o. H2 cl2 2hcl 184 кдж. Fecl2 kmno4 hcl.
Zn+hcl zncl2+h2 окислительно-восстановительная реакция. По термохимическому уравнению h2 cl2 2hcl 184. 36. Fe+2hcl fecl2+h2. Задачи на термохимию.
H2 cl2 2hcl 184 кдж. Fe nh3 h2o. Реакция окисления аммиака. Аммиак и кислород реакция. I2 cl2 h2o.
H2+cl2 hcl. H2 cl2 2hcl 184 кдж. Fecl2 kmno4 hcl. H2 cl2 2hcl 184 кдж. H2 cl2 2hcl 184 кдж.
H2 cl2 2hcl 184 кдж. Cl2 hcl nacl agcl осуществить превращения. 36. H2 cl2 2hcl 184 кдж. Реакция h2 +cl2=2hcl +184,6 кдж является:.